Трансплантация костного мозга (ТКМ) или трансплантация гемопоэтических стволовых клеток (ТГК) — это сложная медицинская процедура, часто применяемая с целью терапии патологий красного костного мозга, некоторых заболеваний крови при прогрессирующих течениях онкологического спектра. Суть метода заключается в пересадке стволовых клеток крови, способных к кроветворению, от донора к реципиенту, нуждающемуся в трансплантации.
[obvodka]
- Физиология кроветворения
- Показания к трансплантации
- Виды пересадки костного мозга
- Подготовка реципиента и донора
- Техника проведения ТКМ
- Восстановление после ТКМ
- Прогноз
[/obvodka]
Краткая физиология кроветворения
Система крови человека, как и других теплокровных млекопитающих, представляет собой сложную морфологическую, взаимозависимую структуру, определяющую не только функциональные задачи питания и иммунной защиты всего организма. Она играет и жизнеопределяющую роль в целом.
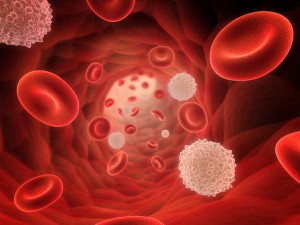
Кровь является основной биологической жидкостью организма, состоящей из жидкой ее части, плазмы, и клеток крови, разделенных по своим морфологическим и функциональным характеристикам. Несмотря на ее физически жидкое состояние, кровь относят к разновидности тканей, которая, в отличие от «твердых» аналогов, содержит свои клетки в динамическом состоянии. Кровь человеческого организма определяет определенный клеточный состав форменных элементов.
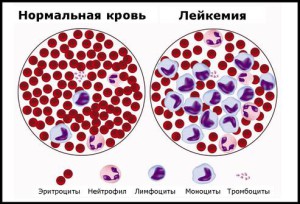
Эритроциты или красные кровяные тельца — самая многочисленная структура среди всех форменных элементов крови. Они представляют собой округлые клетки двояковыпуклой формы и в своем составе (в преобладающих количествах) содержат железофильный белок гемоглобин, который и определяет красный цвет крови. Основная роль эритроцитов в транспортировке газообразных химических веществ, т. е. кислорода к клеткам организма и углекислого газа — от них, тем самым обеспечивая дыхательные функции живых клеток.
[obvodka]Кроме обеспечения кислородной трофики тканей, эритроциты участвуют в передаче других энергетических компонентов, белков, жиров и углеводов в клетки тканей и органов, а также выводят из них продукты метаболизма.[/obvodka]
Лейкоциты — это большая группа белых клеток крови, обеспечивающих иммунные (защитные) свойства организма против чужеродных агентов, т. е. инфекционных телец, аллергических компонентов и других. Это единственные представители форменных элементов крови, способные покидать русло кровеносных сосудов и организовывать иммунную защиту в межклеточном пространстве.
В зависимости от морфологических особенностей и выполняемых задач, лейкоциты разделяют на:
- гранулоциты — нейтрофилы, эозинофилы и базофилы;
- агранулоциты — лимфоциты и моноциты, которые характеризуются крупными размерами своих представителей.
Каждый вид лейкоцита выполняет задачи, возложенные на него природой.
- Блокирование продуктов жизнедеятельности патогенного агента.
- Выработка веществ, способных вызвать его деструкцию.
- Физический захват и поглощение, данный процесс называется фагоцитозом.
Количество лейкоцитов в общем кровяном русле всегда неоднозначно. У физиологически здорового организма с нормально развитым состоянием иммунитета концентрация белых клеток крови увеличивается в период болезни и под воздействием аллергенов различной природы. Однако стоит учесть, что во время отсутствия сложных патологических состояний общее количество лейкоцитов должно оставаться в нормологических пределах. Для исследования концентрации и видового наполнения белых клеток крови, проводится лабораторное исследование крови — лейкоцитарная формула.
Тромбоциты или кровяные пластинки, чаще плоской формы клетки, способные к обеспечению свертываемости крови в местах повреждений наружных кожных покровов или других поражениях кровеносных сосудов, различной сложности. Благодаря тромбоцитам, происходит кровоостанавливающий эффект,путем образования тромба в местах повреждений сосудов, что обуславливает защиту от потери крови.
При поступлении сигнала о том, что в определенном месте произошло нарушение целостности кровеносного сосуда, к нему устремляется огромное количество тромбоцитов, которые совместно с белками плазмы крови организуют процесс ее свертывания.
[plus title=’Каждому виду клеток крови присущи свои сроки жизни.’]
- «Долгожителями» считаются эритроциты — каждая клетка этого ряда проживает срок около 120 дней, после чего гибнет, а на ее место приходит другая.
- Тромбоциты не теряют своей полезной функциональности в течение 10 дней.
- Лейкоциты — около 3-4 дней.[/plus]
Их этого следует, что система крови должна поддерживать свой баланс соотношения и количественных характеристик всех видов крови. Таким образом, на протяжении всей жизни человека происходит регулярное и последовательное замещение отслуживших клеток крови на новые, готовые в полной мере выполнять свои задачи. Процесс обновления клеток крови называется гемопоэзом или кроветворением.
В гемопоэзе участвуют отдельные органы и ткани, способные к зарождению и последующему формированию различных клеток крови. Такими органами являются красный костный мозг, селезенка и печень. Стоит отметить, что кроветворные функции печени имеют место лишь от рождения и в период раннего детского возраста. С каждым годом взросления эти функции печени идут на спад и полностью исчезают.
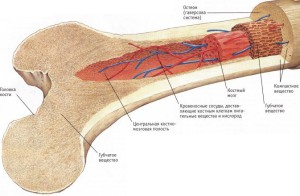
Также не постоянны кроветворные функции красного костного мозга, анатомически заключенного в просвете крупных трубчатых костей нижних конечностей и тазового пояса — основных скелетных формирований, содержащих продуктивный красный костный мозг. По достижению 20-летнего возраста постепенно снижаются гемопоэтические функции красного костного мозга, это случается по причине его перерождения в жировую ткань — желтый костный мозг.
Селезенка — единственный орган кроветворения, который практически не теряет своих продуктивных качеств в отношении производства кровяных телец. Анатомически орган представлен двумя областями — красной пульпой, где образуются эритроциты, и белой, где зарождаются другие форменные элементы крови.
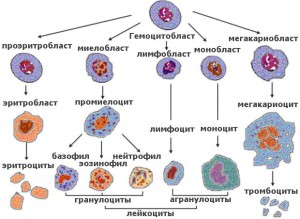
Уникальной особенностью кроветворения является тот факт, что любой вид клеток крови, независимо от их анатомических характеристик и физиологической функциональности, преобразуется из одного единственного вида — стволовой кроветворной (гемопоэтической) клетки. В результате множественного деления и морфологических трансформаций, из стволовой клетки образуются два вида клеток второго ряда — лимфоидные клетки-предшественницы лимфоцитов и миелоидные клетки, из которых в дальнейшем образуются остальные форменные элементы крови.
Процесс кроветворения является очень сложной, генетически обусловленной и зависимой от большого числа внешних и внутренних факторов, системой. Такие обстоятельства зачастую создают условия, нарушающие нормальное кроветворение. Однако при достаточном уровне физиологически здоровой обеспеченности компенсаторные системы организма, особенно в молодом возрасте, способны быстро изменять ситуацию в положительном направлении. По достижении среднего и зрелого возраста, в силу снижения продуктивности органов кроветворения и общего старения органов и тканей, качество и скорость гемопоэза значительно снижаются, тем самым, обуславливая риск кроветворных осложнений.
Клетки крови, достигшие предела своей функциональности, обезвреживаются и уничтожаются в печени.
Что такое костный мозг и показания для его трансплантации
Как уже отмечалось, одним из основных органов кроветворения является костный мозг, а именно красная его часть. Учитывая, что красный костный мозг является местом зарождения всех видов форменных элементов крови, принято говорить не только о его функции гемопоэза, но и иммунопоэтических характеристиках.
[obvodka]Характерным отличием костного мозга от других органов кроветворения является уникальность в производстве первичных стволовых гемопоэтических клеток. В остальные кроветворные органы эти клетки поступают в нативном виде с током крови, и только после в них образуются лимфоидные и миелоидные клетки второго ряда.[/obvodka]
Большая часть кроветворно способной ткани красного костного мозга находится:
- внутри полостей тазового отдела костной основы скелета;
- несколько меньше его в эпифизах длинных трубчатых костей;
- еще меньше его внутри позвонков.
Биологически красный костный мозг защищен от воздействия собственных иммунных клеток так называемым барьером иммунологической толерантности, который препятствует проникновению в паренхиму мозга собственных белых клеток крови.
Первичные стволовые кроветворные клетки способны к неограниченному делению, тем самым обуславливая множественное образование разных форменных элементов из одной первичной стволовой клетки. Такая уникальная особенность создает некоторые условия слабой устойчивости стволовых клеток к воздействию агрессивных воздействий, в частности, химического и лучевого. Поэтому во время лечения онкологических патологий в первую очередь нарушаются процессы в системе кроветворения и иммунной защите.
Пересадка или трансплантация костного мозга -это относительно молодой способ терапии патологических состояний, вызванных недостаточностью кроветворения, которые в ранней хирургии считались неизлечимыми. Годом рождения ТКМ считается 1968-ой, когда впервые было проведена пересадка костного мозга у человека.
На сегодняшний день ТКМ проводится при большинстве онкологических и гемопоэтических патологий, а также при нарушениях иммунного ответа организма.
Показаниями для трансплантации костного мозга могут явиться разные заболевания
- Лейкоз, или рак крови.
- Апластическая анемия.
- Лимфомы различного генеза.
- Множественные миеломы.
- Осложненные состояния иммунитета.
- Злокачественные новообразования различных органов и тканей.
Все патологии, требующие ТКМ, как правило, объединены одной характеристикой. Во время разрушения или нарушения функциональности костного мозга происходит активная выработка им большого количества незрелых и дефективных форменных элементов крови, как правило, белого ряда. Данные нефункциональные клетки заполняют собой кровеносное русло, все больше вытесняя концентрации здоровых аналогов. Чаще всего дефицит затрагивает именно белые кровяные тельца, которые, как известно, отвечают за иммунные защитные характеристики. Таким образом, общее качество иммунитета понижается, что способствует развитию вторичных патологий, как правило, инфекционного ряда. Без применения ТКМ такие процессы носят прогрессирующий характер и быстро приводят к скоропостижному летальному исходу.
Индивидуальные показания для ТКМ определяются только группой лечащих специалистов.
Необходимо отметить, что пересадка непосредственно костномозговой ткани использовалась на ранних этапах применения этой медицинской процедуры. В арсенале современной хирургии существует несколько разновидностей ТКМ, когда вмешательство в анатомическую и физиологическую целостность красного костного мозга не производится. Однако, в силу исторического обоснования, все процессы по перемещению из организма в организм стволовых гемопоэтических клеток носят общее называние — «трансплантация красного костного мозга».
Виды пересадки костного мозга
Как уже упоминалось, трансплантация костного мозга может быть представлена несколькими возможными хирургическими методами.
- Трансплантация непосредственно костного мозга, когда у донора забирают не более 5% костного мозга из костей тазовой области.
- Трансплантация стволовых клеток периферической крови (ТПСК) — забор стволовых клеток представляет классическое взятие крови из вены.
- Трансплантация пуповинной крови (ТПК) — в момент рождения ребенка собирают кровь из перерезанной пуповины. Такая кровь наиболее богата стволовыми клетками первого и второго ряда.
Красный костный мозг, используемый для последующей трансплантации, может быть получен у самого пациента или других людей.
[plus title=’Существует несколько видов трансплантации костного мозга.’]
- Аллогенная трансплантация, когда донорский материал получен не от родственника пациента.
- Сингенная трансплантация — красный костный мозг взят у близкого родственника пациента, как правило, кровных сестер или братьев.
- Аутологическая трансплантация — донорский материал, полученный у самого пациента, очищен от патологических агентов, дефективных клеток и заново введен внутривенно. Возможностей для использования аутологической трансплантации, как правило, мало. Это возможно только на стадиях ремиссии заболеваний или при патологиях, не затрагивающих красный костный мозг, например, при новообразованиях других органов.[/plus]
Учитывая ее первичную неоднородность и способность к множественной трансформации, пересадка гемопоэтических клеток представляет собой достаточно сложный процесс. Ведь донорский материал должен подходить не только на уровне группы крови и резус-фактора, но и максимально соответствовать генетическому сходству с клетками реципиента. Поэтому этап подбора донора является самым сложным и долговременным во всем процессе лечения.
Особенно ситуация ухудшается с отсутствием у пациента близких, кровных родственников, в этом случае приходится прибегать к аллогенному типу трансплантации. С этой целью многие страны мира предоставляют свои базы доноров, где указаны необходимые данные для пересадки. Самой большой базой владеет США, на втором месте — Германия. К сожалению, в нашей стране подобная донорская база носит рассеянный, очаговый характер и включает в себя достаточно малое количество доноров.
Этапы подготовки пациента и донора костного мозга
Процедура трансплантации костного мозга требует длительной и усиленной подготовки. Как уже говорилось выше, необходимо соответствие не только морфологических характеристик крови между донором и пациентом (группа крови), но и их генетическая структура должна быть максимально сходной.
[obvodka]По данным Международной ассоциации доноров костного мозга (МАДКМ) за 2007 год, от 1430 потенциальных доноров благополучная пересадка возможна лишь одному реципиенту. Речь идет об аллогенной трансплантации.[/obvodka]
Донором костного мозга может стать абсолютно любой человек.
- В возрасте от 18 до 55 лет
- В анамнезе потенциального донора не должно быть гепатитов В и С, туберкулеза, малярии, онкологических заболеваний, психопатологических состояний и расстройств.
- Донор не может быть носителем ВИЧ-инфекции и других серьезных диагнозов, заранее оговоренных в договоре о сдаче донорского материала.
После исследования физиологического здоровья потенциального донора проводится исследование на систему генов тканевой совместимости или человеческого лейкоцитарного антигена (англ. HLA, Human Leucocyte Antigens) — HLA-типирование. Суть метода заключается в определении генетических характеристик, которые позволят в последующем сравнить их с аналогичными данными у реципиента. Для типирования требуется не более 10 мл крови, взятой из вены.
Перед непосредственной трансплантацией пациента подвергают так называемому кондиционированию, тяжелой медицинской процедуре, направленной на:
- практически полное уничтожение красного костного мозга, не способного в полной мере реализовывать свои гемопоэтические функции;
- подавление иммунных сил организма путем уничтожения остаточных белых кровяных телец в периферической крови, печени и селезенке. Проводятся эти манипуляции с целью предупреждения атаки родных иммунных клеток на чужие донорские материалы.
Стоить отметить, что процесс кондиционирования является необратимым и, в случае неудачной трансплантации, пациента ждет летальный исход в любом случае.
Этап кондиционирования проводится в асептических условиях интенсивной терапии с помощью активного воздействия на организм методов химиотерапии или облучения. Зачастую используются оба этих способа с целью максимально быстрого подавления иммунитета и деструкции костного мозга. В процессе кондиционирования пациенту вводятся артериальные и венозные катетеры, предназначенные для регулярного забора крови на предмет мониторинга состояния клеточного состава и введения химических веществ. Стоит отметить, что дозировки химиотерапевтических препаратов существенно превышают таковые в онкологической практике. Поэтому пациенты, как правило, находятся в стабильно тяжелом состоянии, осложненном нарушениями нервной, пищеварительной и мочеполовой системы.
Общая продолжительность этапа кондиционирования длится от 2 до 5 дней, в зависимости от общего состояния пациента и изменения его видового состава крови.
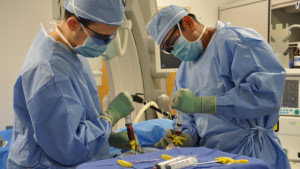
Техника проведения операции по трансплантации костного мозга
Для донора механизм проведения операции по трансплантации костного мозга не представляет сложности и не особенно болезненный. Современная трансплантология крайне редко прибегает к забору материалов непосредственно из мест расположения костного мозга, благодаря наличию медикаментозных средств, стимулирующих массовый выход стволовых гемопоэтических клеток в периферическую кровь.
Сама процедура получения материала напоминает процесс переливания крови. К кровеносной системе донора подключают специальную аппаратуру забора, которая постепенно получает необходимые порции крови, параллельно проводя отделение стволовых клеток от общего количества иных форменных элементов крови — аферез. После чего обработанная кровь вновь возвращается в организм.
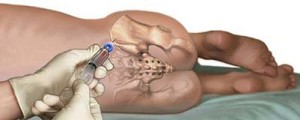
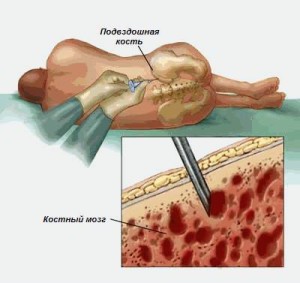
Если при определенных показаниях требуется непосредственный забор донорского материала из просветов трубчатых костей, донора необходимо госпитализировать на день. Процесс получения стволовых клеток крови проводится вместе с остальными клетками красного костного мозга под общей анестезией, ведь он довольно болезненный.
Забор производят из нескольких мест в районе тазовых костей специально предназначенными для этого шприцами, оборудованными длинными иглами с широким просветом. Время процедуры занимает не более двух часов. Общее количество полученной массы костного мозга составляет не более 2 л. Несмотря на довольно значительные объемы, после фильтрования остается не более 1 % полезного объема суспензии, содержащей гемопоэтические стволовые клетки. Как правило, физиологические объемы костного мозга восстанавливаются в течение 1-2 месяцев.
[obvodka]Процесс пересадки для реципиента отличается своей простотой и безболезненностью. Донорская суспензия стволовых клеток вводится классическим внутривенным способом в условиях палаты интенсивной терапии.[/obvodka]
В качестве материала может быть использована суспензия, только что полученная от донора, либо взятая некоторое время назад и замороженная с целью длительного хранения. В замороженном виде чаще хранят трансплантаты, взятые в местах географического удаления, либо при использовании пуповинной крови.
Восстановление после операции и РТПХ после пересадки костного мозга
Безусловно, риску осложнений в процессе трансплантации доноры подвержены в гораздо меньшей степени. Характерными последствиями забора костного мозга, независимо от его методов, являются:
- боли в костях;
- общая слабость;
- возможны проявления аллергических реакций.
Такая симптоматика связана, прежде всего, с применением препаратов, способствующих активной выгонке стволовых клеток в периферическую кровь. Статистические исследования указывают на 0,6 % от общего числа доноров, которым потребовалась длительная госпитализация, связанная с нарушением восстановления системы крови. Летальных исходов, как и повышения онкологического риска, среди этого количества не отмечено.
Что касается пациента, то риск осложнений достаточно велик в силу генной разнородности донорского материала и собственного организма. Широко известен феномен так называемой реакции «трансплантат против хозяина» (РТПХ), возникающий у 97 % пациентов из общего числа реципиентов стволовых клеток крови. Такое осложнение связано с восприятием пересаженными белыми клетками крови окружающих тканей как чужеродных патологических агентов, против которых они начинают вести усиленную борьбу.
РТПХ проявляется разной степенью тяжести, что зависит от величины разности генетического несоответствия. Но, в любом случае, такое явление имеет место быть. Подобрать 100 % генного соответствия невозможно. Клинически симптоматика РТПХ проявляется в виде поражения:
- кожных покровов;
- слизистых оболочек;
- пищеварительной системы.
В этот период практически полностью отсутствуют защитные силы организма, что способствует быстрому заражению пациента любой инфекцией, в том числе и латентно скрытой до того момента, когда возникла необходимость в трансплантации.
Поддержка организма в период РТПХ проводится с помощью препаратов, подавляющих иммунитет, деятельность белых кровяных телец.
Кроме тяжелого физического состояния, пациент испытывает серьезный эмоциональный дискомфорт, вызванный осознанием возможной смерти вследствие возможно неизлечимой болезни. Ситуацию усугубляют перемежающиеся ощущения общего состояния, ведь для восстановительного периода характерны частые перепады улучшений и ухудшений. На восьмой день после операции пациент может себя физически хуже чувствовать, нежели чем на последующий после трансплантации день.
После выписки, которая, как правило, происходит на 2-4 месяц после трансплантации, пациент должен регулярно посещать лечебное учреждение около полугода с целью продолжения амбулаторной терапии и переливаний крови, если того потребует его состояние реабилитации. За это время белый состав его крови еще не достигает необходимой концентрации, что обуславливает достаточно низкий уровень его иммунитета. По причине высокой восприимчивости к инфекционному заражению больным запрещено посещать места массового скопления людей и совершать иные действия, которые могут вызывать общее переохлаждение организма.
Полное восстановление системы крови происходит, как правило, через 2-3 года после выписки.
Прогноз после операции ТКМ
Уровень летальности с момента установления диагноза, требующего пересадки костного мозга, до завершения периода РТПХ равнозначен и составляет около 50 % при условии удачной трансплантации. Если операция по пересадке стволовых клеток крови не была проведена, пациенту отводится достаточно малый срок жизни. Поэтому при появлении такой возможности ТКМ нужно проводить в любом случае.
Прогноз успешности ТКМ зависит от многих факторов.
- Степень генной однородности по системе HLA-типирования — чем выше ДНК-сходство донора и реципиента, тем лучше.
- Стабильность пациента до пересадки — если его первичное заболевание находилось в статичном состоянии или стадии ремиссии, то прогноз будет более благоприятным.
- Возраст пациента напрямую характеризует качество приживаемости донорских стволовых клеток — в молодые годы этот показатель заметно выше.
- Во время или после трансплантации у пациента не должно появиться сложных вирусных инфекций, особенно вызванных родом цитомегаловирусов.
- Повышенная концентрация нативных стволовых клеток в донорском материале повышает шансы на благоприятный исход, однако способствует высокому риску осложнений при РТПХ.
- Соотношение выживаемости находится на уровне 90 %, если поводом для пересадки послужили патологии неонкологического спектра, при условии введения донорского материала, взятого у самого пациента или его родственника, и до 65 % — у других людей.
В заключение хотелось бы отметить, что, несмотря на долгий подбор донорского материала, тяжесть реабилитационного периода и достаточно низкий процент благоприятного исхода, все пациенты, пережившие свои смертельные болезни, не сожалеют ни на минуту о тяжестях, связанных с процессом пересадки.